RACE
Dear Health Care Professionals,
Gilead Sciences has always committed to drive innovation and improve patient lives and our ongoing focus is to advance viral hepatitis research, education and share best practices to achieve global elimination and cure. Undoubtedly, the RACE to beat viral hepatitis involves not only patients themselves, but the collaborative effort of the medical professionals, scientists, government and pharmaceutical industries. This monthly e-newsletter is a scientific platform for the Gilead Medical Affairs team to update you on recent advances and global innovative effort made to propel us to the next level. We hope it will spark up some interesting discussion among us.
Gilead Medical Affairs team

大師觀點
關注腎移植病人的 HBV 再活化風險
掌握肝功能與評估預防治療缺一不可
專訪 蔡炘儒 醫師 / 台中榮民總醫院胃腸肝膽科

- 康復型 B 肝感染(resolved HBV infection)的腎移植受贈者(kidney transplant recipients)仍有 HBV 再活化(hepatitis B virus reactivation, HBVr)風險,建議每 3 個月定期監測 AST(aspartate aminotransferase)/ALT(alanine aminotransferase)以及每 6 – 12 個月追蹤 HBsAg(hepatitis B surface antigen)。
- 腎移植受贈者於高劑量類固醇調降的 1 年內發生 HBVr 的風險較高,建議這段期間密切監測肝功能和 HBsAg。肝功能異常者,需進一步檢驗 HBV DNA。
- 第一線 B 肝口服抗病毒藥物(nucleos(t)ide analogues, NAs)均可有效抑制 HBV,用藥選擇以安全性為主要考量。
- 新興免疫抑制劑和生物製劑的 HBVr 風險未知,建議臨床醫師定期監測 B 型肝炎各項指標。
臨床新訊
康復型 B 肝感染者
於接受腎移植後的 HBV 再活化風險評估 1
- 慢性 B 肝感染或康復型 B 肝感染者在腎臟移植後,均有 HBV 再活化(HBVr)風險,可能導致肝臟病變或死亡。
- 台灣回溯型世代研究顯示,康復型 B 肝感染的腎移植受贈者若為 anti-HBs(-)、每日平均類固醇劑量增加,以及最大類固醇劑量 ≥ 20 mg/day prednisolone 等價當量,均有較高 HBVr 的發生風險。
- anti-HBs(-) 和高劑量類固醇均為 HBVr 的獨立危險因子。最大類固醇劑量 ≥ 20 mg/day prednisolone 等價當量的病人,10 年 HBVr 累積發生率可達 13.1%。帶有 2 項風險因子的病人,10 年 HBVr 累積發生率超過四成。
- 儘管感染 HBV 不一定會直接導致腎臟病變,但 B 肝惡化卻可能成為腎移植受贈者(kidney transplant recipients, KTRs)發病或死亡的主要原因。有慢性 B 肝(CHB)的腎移植病人可能因使用免疫抑制治療導致肝纖維化快速惡化,進而死於肝臟相關併發症。
- 康復型 B 肝感染者(anti-HBc(+) / HBsAg(-), resolved HBV infection)發生 B 肝惡化的風險雖然較 HBsAg(+) 病人低,但潛伏體內的 HBV 仍可能在病人免疫系統被抑制時再活化(HBVr)。過去研究顯示這類病人在腎移植後的 HBVr 發生率約為 2 – 9.6%,無 anti-HBs 抗體者的 HBVr 發生率更高,然而現行指引僅建議定期回診觀察,而非長期給予 B 肝口服抗病毒藥物(NAs)作為預防治療。
- 目前還不十分清楚康復型 B 肝感染者在腎移植後,使用免疫抑制治療的 HBVr 發生風險(特別是不同劑量或療程的類固醇),因此有必要釐清腎移植受贈者發生 HBVr 的時機、嚴重度與可能的危險因子,以避免此類病人發生嚴重的肝臟併發症。
- 台中榮民總醫院執行一項以醫院為基礎的回溯型世代研究,納入 2000 – 2020 年共 257 位 anti-HBc(+) 腎移植受贈者的病歷資料, 以 anti-HBs 有無分為 2 組,分析免疫抑制劑在誘導治療(rituximab、basiliximab、thymoglobulin 等)以及標準三合一維持療法(包括 CNI、MMF、類固醇)期間發生 HBVr 或 HBV 相關肝炎的情形。

- 兩組病人的基線期特徵一致,和 anti-HBs(-) 病人相比,anti-HBs(+) 病人的平均年齡較低(49 歲 vs 51.5 歲,P = 0.008)。兩組均有 > 85% 病人使用 tacrolimus + MMF + 類固醇三合一維持療法,類固醇平均劑量(6.0 – 6.1 mg/day)與最大劑量的病人比例也相近;anti-HBs(+) 病人有較多比例併用 sirolimus 或 everolimus,但未達統計差異(45.3% vs 28.9%,P = 0.064)。兩組均有 > 65% 病人無發生急性排斥反應。
- 追蹤 10 年的數據顯示,anti-HBs(-) 病人無論是 HBVr 或肝炎發作(hepatitis flare)的累積發生率,均顯著高於 anti-HBs(+) 病人(圖一)。
圖一、康復型 B 肝感染的腎移植受贈者 HBVr 與肝炎發作累積發生率
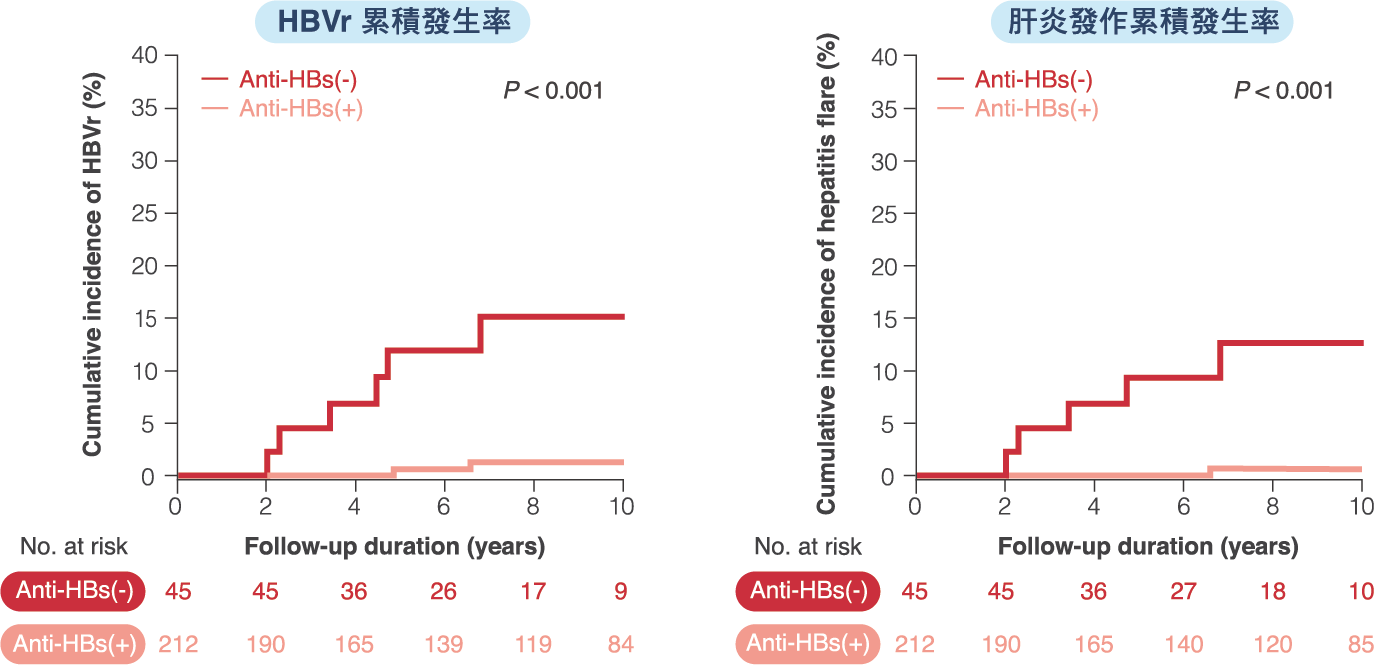
- 追蹤期間共有 8 位病人發生 HBVr,其中 6 位為 anti-HBs(-),2 位為 anti-HBs(+),約在腎移植後 2 – 6 年、以及類固醇自最大劑量調降的一年內發生 HBVr(表一)。
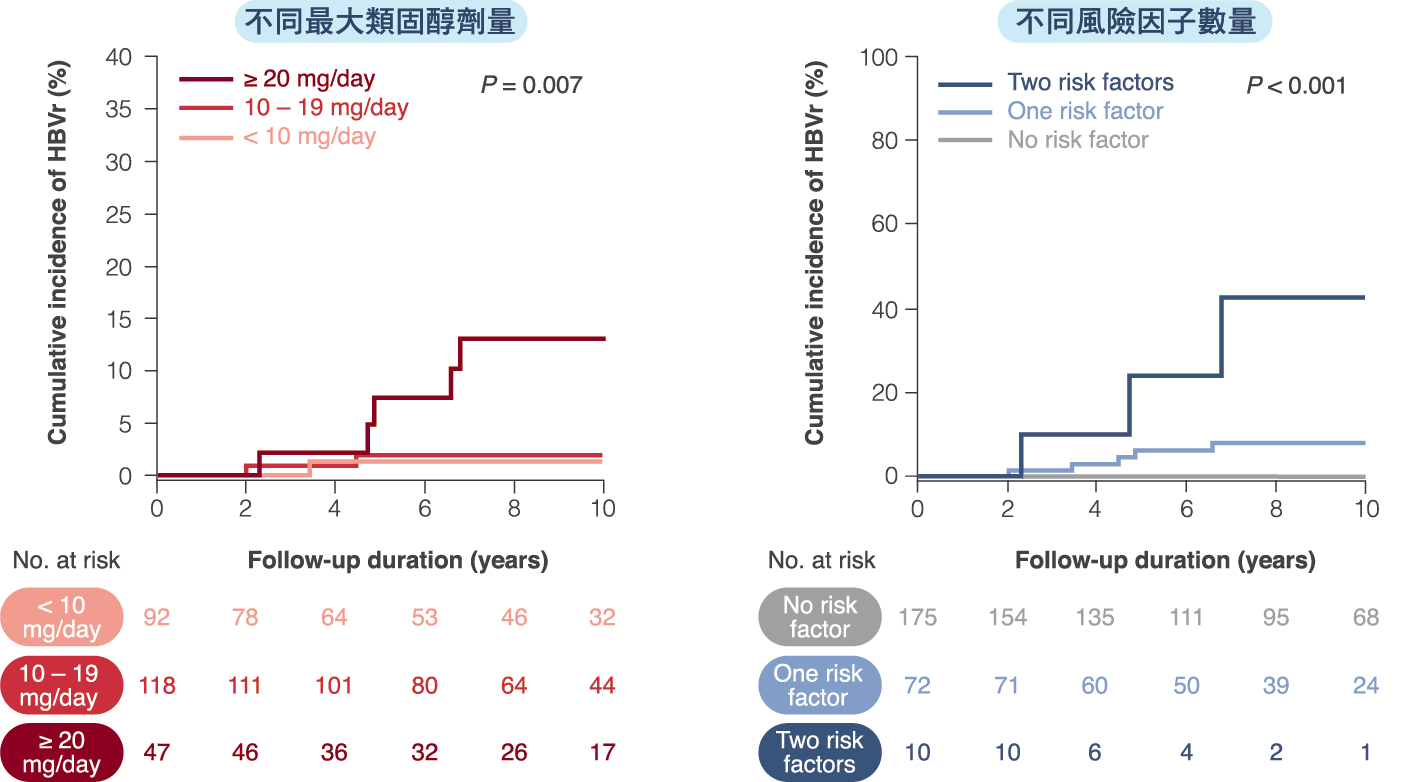
- 根據多變項迴歸分析結果,anti-HBs(-) 和高劑量類固醇均為 HBVr 的獨立危險因子。最大類固醇劑量 ≥ 20 mg/day prednisolone 等價當量的病人,其 10 年 HBVr 的累績發生率可達 13.1%;而帶有 2 種、1 種和無風險因子的病人,10 年 HBVr 的累積發生率分別為 42.7%、7.9%、0%(圖二)。
圖二、康復型 B 肝感染的腎移植受贈者 HBVr 累積發生率

臨床新訊
Belatacept* 用於腎移植病人
有高度 HBV 再活化風險 2
* Belatacept 未在台上市
- 腎移植受贈者有較高的 HBV 感染盛行率,在法國約有 1.4% 的腎移植受贈者為 HBsAg(+),而這些病人通常在腎移植後的預後較差,死亡率約為 HBsAg(-) 病人的 2.49 倍;而過去文獻也顯示,anti-HBc(+) / HBsAg(-) 的腎移植受贈者仍有 3 – 9% 會發生 HBVr。
- Belatacept 是一種共同調節阻斷劑(costimulatory blockade agent),藉由與抗原呈現細胞(APCs)表面的 CD80 與 CD86 相結合,阻斷 APCs 經由 CD28 活化 T 細胞的路徑。此藥常與類固醇和 MMF 併用於腎移植受贈者,作為 CNI 的替代藥物。然而目前尚無研究探討此藥物在腎移植受贈者的 HBVr 風險。
- 一項由法國 2 間移植中心執行的回溯型世代研究,納入 1993 年 7 月至 2019 年 7 月 135 位腎移植受贈者,分析使用 belatacept 後的病人存活率、移植腎存活率,以及 HBVr 情形與相關風險因子。
- 接受 belatacept 治療的腎移植受贈者無論是 anti-HBc(+)(n = 32)或是 anti-HBc(-)(n = 103),移植後病人存活率與移植腎存活率均沒有顯著差異。
- anti-HBc(+) 病人中有 7 位(21.9%)發生 HBVr,其中 2 位為 HBsAg(+),平均發生時間為移植後 54.8 個月。然而 HBVr 並不影響病人存活率與移植腎存活率。單變項迴歸分析也顯示沒有任何風險因子(包含 HBsAg(±)、是否給予 B 肝抗病毒預防治療)與 HBVr 的發生有關。

精華回顧
台灣前瞻型研究:腎移植 CHB 病人改用 TAF 後療效與遵醫囑性良好,腎功能維持穩定 3
- 腎移植的 CHB 患者改用 TAF 治療 24 週後,可有效抑制 HBV DNA,並顯著提升 ALT 值恢復正常的病人比例。在 TAF 治療期間,病人的 eGFR 維持穩定,用藥遵醫囑性高達 96.4%。
- 有鑑於 TAF 用於腎移植 CHB 病人的療效與安全性數據較為有限,台中榮民總醫院進行一項前瞻型世代研究,納入 30 位腎移植的 CHB 感染者,觀察改用 TAF 治療 24 週的療效、安全性與遵醫囑性。
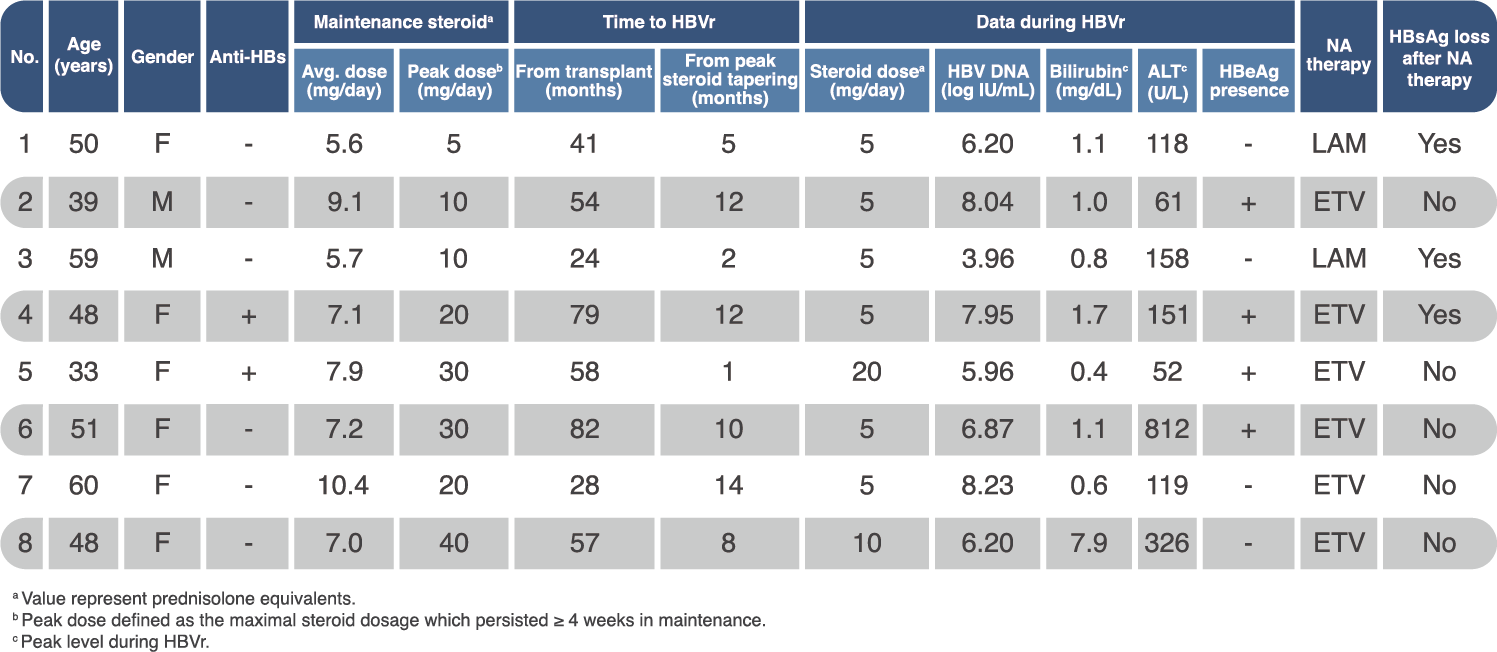
- 30 名受試者的中位年齡為 58.5 歲,其中 27 位在轉換為 TAF 之前是使用 ETV 治療;56.7% 病人為慢性腎臟病(CKD)第 1 – 2 期,43.3% 病人為 CKD 第 3 – 4 期。其它基線期病人特徵請見(表二)。
表二、腎移植的 CHB 病人改用 TAF 治療的基線期特徵
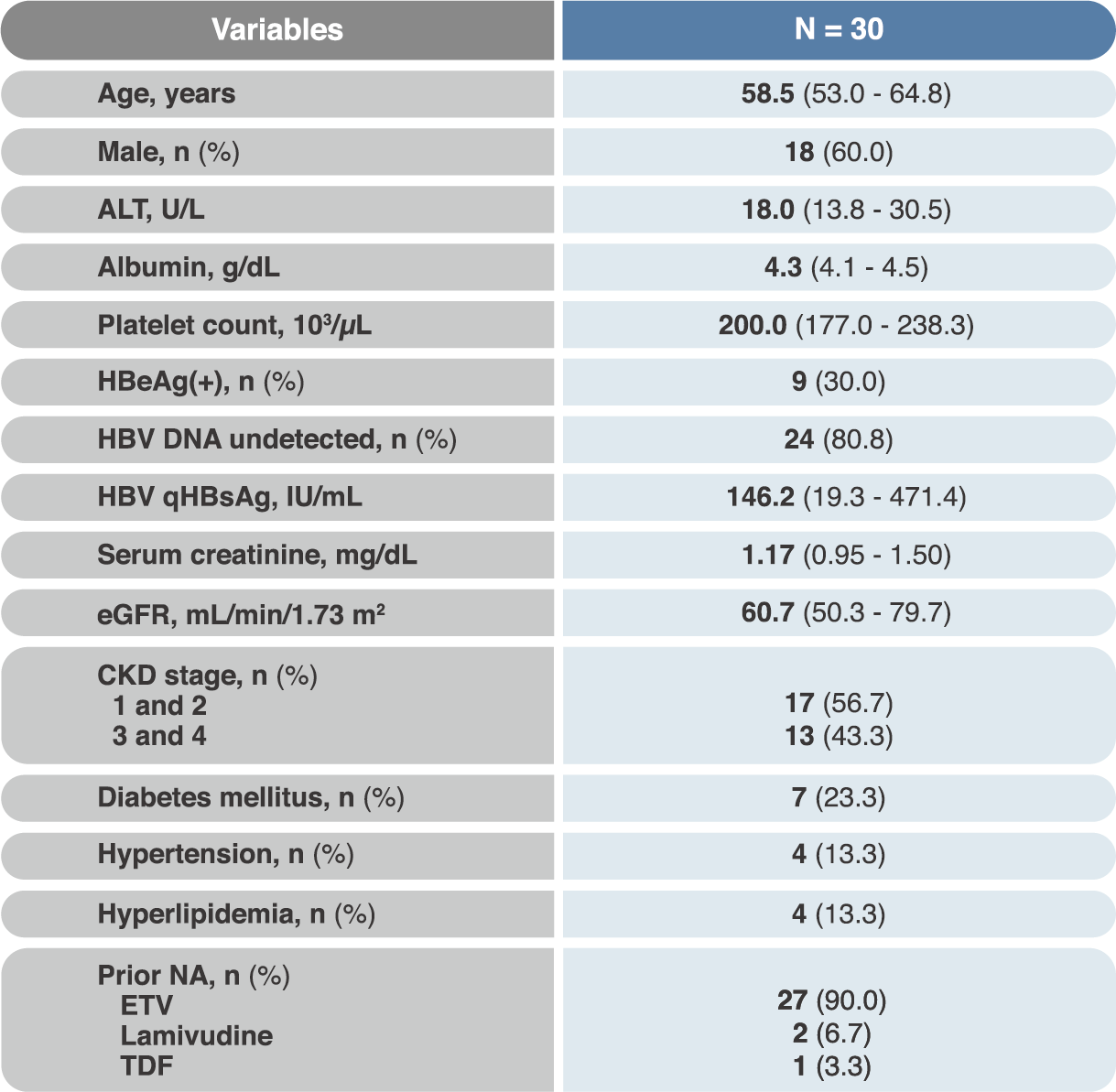
- 轉換為 TAF 後,測不到 HBV DNA 的病人比例從 76.6% 顯著提升至 96.7%(P = 0.014);ALT 恢復正常的病人比例也從 73.3% 顯著增加至 86.7%(P = 0.045)。
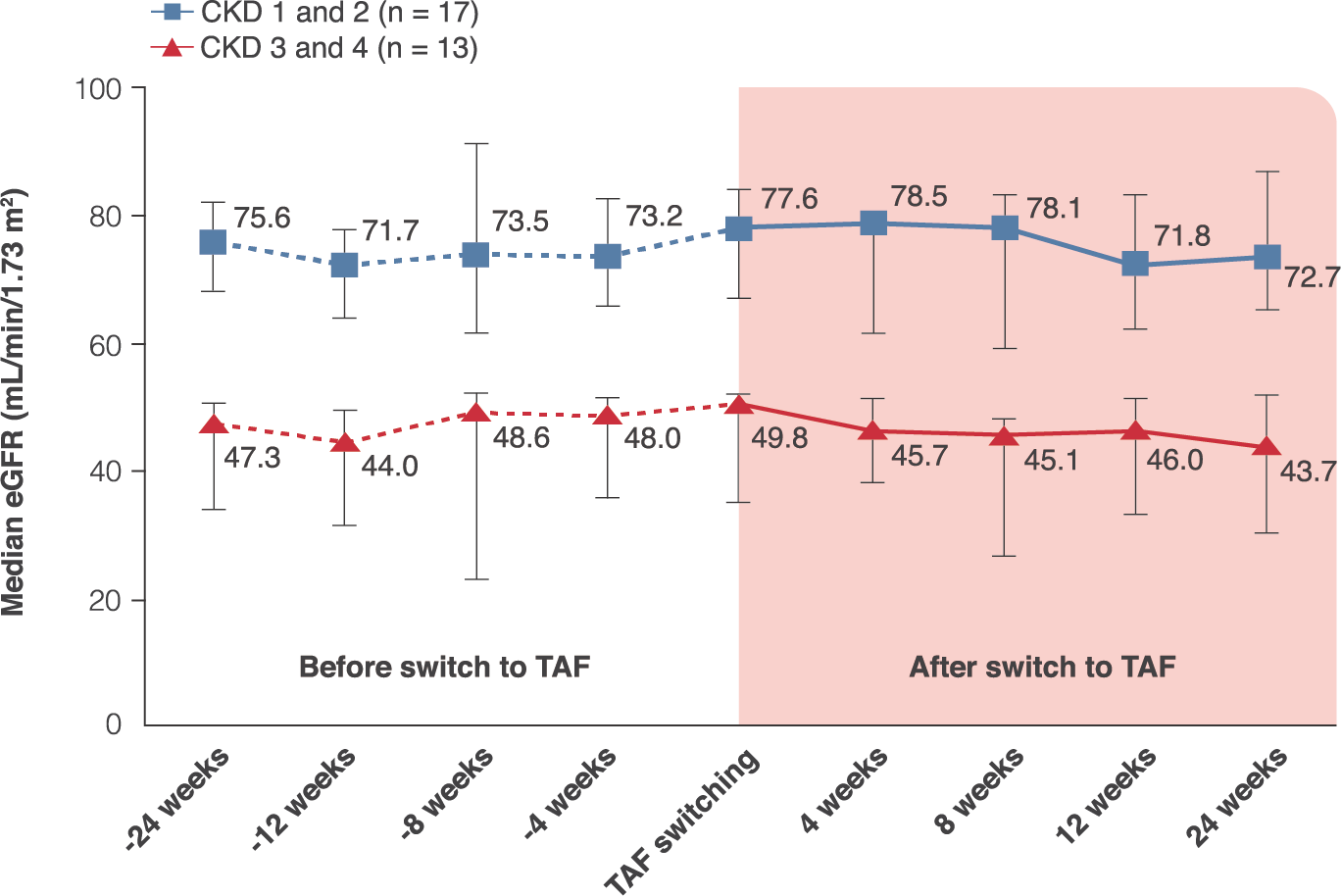
- 在 24 週 TAF 治療期間,不同 CKD 期別病人的腎功能(eGFR)皆維持穩定(圖三);病人的骨密度(BMD)於治療前後也沒有顯著變化(骨小樑評分 1.3 vs 1.4)。
若對文章的內容有任何問題,請您隨時與 Gilead Medical 部門的同仁聯絡。